Identificación de nuevas vulnerabilidades de los tumores BRCA1 resistentes a quimioterapia
Dr. Román González
BRCA1 fue primer gen descubierto, hace ya 30 años, en 1994, cuyas mutaciones conferían predisposición al desarrollo de cáncer de mama. Siendo la principal causa de cáncer de mama hereditario. Ser portadora de una mutación perjudicial en este gen confiere una probabilidad de hasta el 50% de desarrollar cáncer de mama antes de los 50 años y del 90% a lo largo de la vida, siendo además del tipo “triple negativo”, el más agresivo y para el que no existen tratamientos efectivos. Además, mutaciones en BRCA1 también predisponen para la aparición de otros cánceres como el de ovarios o próstata en hombres.
A día de hoy, a las portadoras de mutaciones en BRCA1 se les recomienda la extirpación preventiva de mamas y ovarios para evitar la aparición de cáncer devastador antes de los 50 años de vida.
En estos últimos 30 años son innumerables los estudios y artículos publicados sobre este gen. BRCA1 tiene una función en la reparación de daño en el ADN, en concreto en la reparación de cortes de doble cadena en el ADN, por un mecanismo denominado “recombinación homóloga”. La mayor parte de las terapias mediante radio y quimioterapia buscar producir cortes en el ADN que las células tumorales con este gen mutado no pueden reparar, produciéndoles la muerte. No obstante, mediante mecanismos alternativos estas células desarrollan resistencia a estos tratamientos, dejando de ser eficaces y pasando a ser mucho más agresivos estos tumores.
A pesar de que el gen BRCA1 se conoce y lleva estudiando ya 30 años, el papel de su actividad enzimática E3 seguía siendo controvertido, y aún no se había podido determinar claramente la relevancia en cáncer y reparación de cortes en el ADN, o si estaba implicada en otros procesos. Esto es debido, a que no existían métodos para estudiar directamente la actividad enzimática dentro de las células. Todos los estudios y conclusiones estaban basados en observaciones indirectas, con lo cual no era posible determinar si estas observaciones eran fruto de defectos en la actividad enzimática o efectos colaterales, siendo en muchas ocasiones, resultados contradictorios. Sin embargo, estaba claro que ciertas mutaciones que afectaban a la actividad enzimática y no al resto de BRCA1, predisponían a la aparición de cáncer, siendo estos muchos más agresivos y resistentes a la quimioterapia.
En 2024, mediante una nueva técnica desarrollada en nuestro grupo de investigación, desciframos el papel y la importancia de la actividad E3, y vimos que, si bien es verdad que los tumores BRCA1 deficientes en actividad E3 son resistentes a la quimioterapia empleada en tumores BRCA1, si mueren con otros tratamientos alternativos.
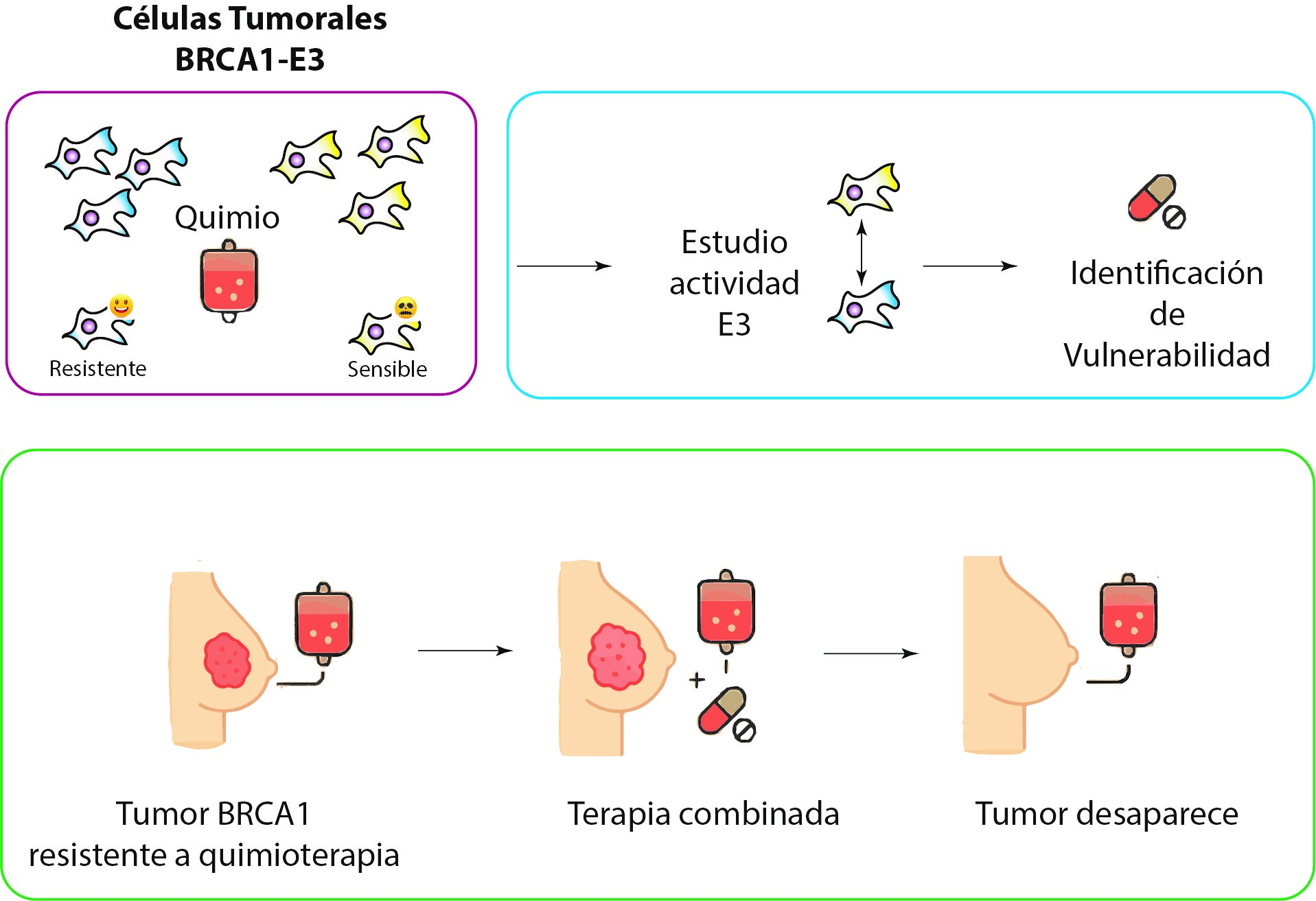
Además, otros grupos de investigación internacionales, has descrito que ciertas células tumorales BRCA1 deficiente en actividad E3 SI son sensibles a la quimioterapia. En este proyecto de investigación pretendemos aplicar nuestros métodos para poder entender por qué la falta actividad E3 hace sensibles a unos tumores a la quimioterapia y a otros no. Así podremos combinar fármacos para hacer sensibles a la quimioterapia a todos los tumores BRCA1 deficientes en actividad E3.
Más información:
Artículo original: https://www.nature.com/articles/s41467-024-48427-6
Artículos de prensa:






